Электрохимические методы очистки вод
Основы электрохимических методов. Для проведения электрохимических процессов используют электролизеры. В простейшем виде это два электрода (электронные проводники), погруженные в раствор электролита (ионный проводник), который находится в ванне. Через электроды пропускают обычно постоянный ток. На катоде, т.е. электроде, подсоединенном к отрицательному полюсу источника напряжения, протекают процессы электрохимического восстановления положительно заряженных ионов раствора, т.е. катионов. На инертном аноде, т. е. электроде, подсоединенном к положительному полюсу источника напряжения, протекают процессы электрохимического окисления отрицательно заряженных ионов раствора, т.е. анионов. На растворимом аноде происходит окисление материала анода с переходом его растворимых соединений в раствор. Процессы электрохимического восстановления и окисления количественно описываются известным законом Фарадея.
В зависимости от природы электрохимических процессов, используемых для удаления примесей из сточных вод, различают методы электрохимического окисления и восстановления, электрокоагуляции и флотации, электродиализа.
Электрохимическое окисление и восстановление. Методы электролиза применяют при небольших расходах сточных вод, содержащих повышенные концентрации примесей. Минимальная концентрация солей должна быть не менее 0,5 г/л, чтобы электропроводность сточной воды была достаточной для электролиза. Анодным окислением можно очищать сточные воды от цианидов, аминов, альдегидов, сульфидов, меркаптанов, красителей, нитросоединений, превращая их в СО2, воду, азот, аммиак. Катодным восстановлением можно удалять ионы тяжелых металлов: свинца, ртути, меди, мышьяка, хрома и т. п.
В качестве анодов применяют нерастворимые материалы: графит, магнетит, титан. Катоды: легированная сталь, сплавы железа, свинца, цинка. Для разделения катодного и анодного пространства применяют керамические, полиэтиленовые, стеклянные диафрагмы. Электропроводность раствора увеличивают добавлением 5-10 г/л NaCl. Анодная плотность тока составляет 100-150 А/м2, межэлектродное пространство — 3 см. Эффективность очистки — до 80-100%.
Электрокоагуляция и электрофлотация
В этом методе используют растворимые аноды из железа (стали), алюминия, которые при анодном окислении образуют ионы Fe3+ и AL3+.
Катионы железа и алюминия: а) коагулируют заряженные коллоиды, б) образуют в воде гидроксиды железа или алюминия в виде хлопьев, в) способствуют соосаждению примесей на них. Если напряжение на электролизере достаточно для параллельного разложения воды, то пузырьки газов водорода H2 и кислорода O2, образующиеся при электролизе на катоде и аноде, будут обеспечивать флотацию примесей. Такие электролизеры с растворимыми электродами называют электрокоагуляционно-флотационными.
Электроды в электролизерах располагают в виде набора пластин с расстоянием между ними для стальных электродов 5-10 мм, для алюминиевых — 12-15 мм. Анодная плотность тока 150-250 А/м2 для стальных электродов и 80-120 А/м2 для алюминиевых электродов. Скорость движения воды между электродами от 0,03 до 0,5 м/с. По направлению движения воды и флотирующихся газов электрофлотаторы разделяют на прямо- и противоточные, по расположению электродов — на горизонтальные и вертикальные.
Электрокоагуляцию с алюминиевыми анодами применяют для обработки сточных вод, содержащих эмульсии масел, жиров и нефтепродуктов с начальной концентрацией не более 10 г/л. Эффективность очистки от масел 55-70%, от жиров до 92-99%. Стальные электроды используют для электрокоагуляции хроматов, тяжелых металлов, фосфатов, полимеров.
Электродиализ
При электродиализе разделение ионов раствора М+ и Х- происходит под воздействием разности концентраций частиц и разности потенциалов, создаваемой в электродиализаторе по обе стороны мембран. Простейший электродиализатор представляет собой ванну, разделенную на три камеры двумя диафрагмами или мембранами (рис. 4.10).
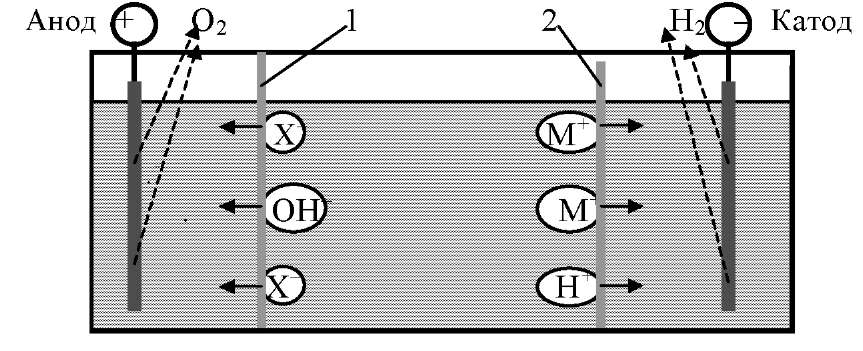
Рис. 4.10. Схема электродиализатора: 1 — анионитовая мембрана;
2 — катионитовая мембрана
В качестве диафрагм используют инертные пористые природные и синтетические материалы: асбест, стеклоткань, полихлорвиниловую ткань и др. В качестве мембран применяют иониты. От средней камеры анионитовая мембрана 1 отделяет камеру с анодом, а катионитовая 2 — камеру с катодом.
При пропускании через электродиализатор постоянного тока на аноде происходит окисление анионов, обычно ОН-, или выделение кислорода при разложении воды:
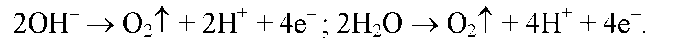
Образующиеся катионы водорода Н+ не могут переходить через анионитовую мембрану в среднюю камеру. Они увеличивают кислотность в анодной камере. Уменьшение концентрации анионов по сравнению с концентрацией катионов ведет к росту разности потенциала и концентрации анионов между анодной и средней камерой. Это увеличивает скорость перехода анионов Х- из средней камеры в анодную камеру через анионитовую мембрану или диафрагму.
Аналогичное явление, но противоположное по знаку, наблюдается в катодной камере, где происходит катодное восстановление катионов водорода или воды:
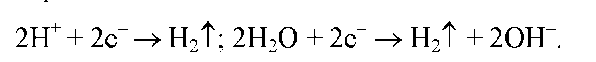
Раствор в катодной камере обогащается ОН--ионами, возрастает его рН, дефицит катионов, разность потенциалов. Ускоряется переход катионов М+ из средней камеры в катодную.
Таким образом, при пропускании через электродиализатор постоянного тока анионы Х- из средней камеры переходят в анодную, а катионы М+ — в катодную камеру, практически до полного их удаления. Применение ионитовых мембран позволяет создавать в анодной камере кислую среду, а в катодной — щелочную. Диафрагмы же не мешают переходу Н+-ионов из анодной камеры и ОН--ионов из катодной камеры в среднюю камеру. В ней они взаимодействуют, образуя воду. Поэтому рН в камерах практически не изменяется.
Аноды и катоды изготавливают из инертных материалов: графита, магнетита, платинированного титана. Число камер в электродиализаторах достигает 100-200. На снижение содержания солей с 250 до 5 мг/л расходуется 7 кВт-ч/м .
